 2026-04-02作者:王玲玲
2026-04-02作者:王玲玲
近日,我校医学部药学院科研团队张志超教授、王紫千副教授等在蛋白靶向降解领域取得重要进展,相关成果发表于《控制释放杂志》(Journal of Controlled Release)和《药物化学杂志》(Journal of Medicinal Chemistry),我校均为唯一通讯单位。
蛋白靶向降解嵌合体技术已发展成为小分子药物开发领域的重要研究范式。然而,该技术存在肿瘤选择性不足、无法实现广域降解覆盖、降解效率受限等问题。对此,团队利用伴侣蛋白在肿瘤发生发展和蛋白质稳态维持中的核心作用,开发了两种基于伴侣蛋白的高效、肿瘤选择性、全域降解覆盖的新型蛋白降解分子,共同构建了一个覆盖更广泛肿瘤谱系、机制互补、模块化设计的蛋白靶向降解技术平台。具体包括:
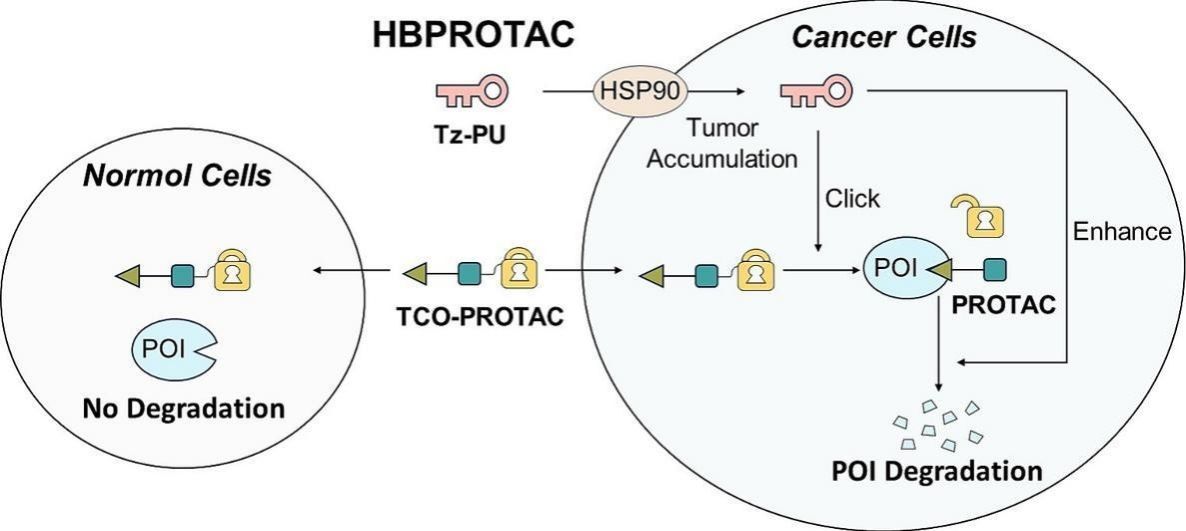
图1.HBPROTAC的机制示意图
靶向HSP90的生物正交PROTAC前药系统(HBPROTAC),不仅在黑色素瘤小鼠模型中实现了PROTAC在肿瘤部位的特异性激活,显著降低全身毒性,还通过HSP90与泛素化-蛋白酶体降解通路的协同作用,增强了靶蛋白的降解效果。相关成果以“HSP90依赖型生物正交PROTAC前药系统实现肿瘤选择性和蛋白质降解增强”(The HSP90-dependent bioorthogonal PROTAC prodrug system enables tumor-selective and enhanced protein degradation)为题发表于《控制释放杂志》(Journal of Controlled Release),我校医学部博士生殷方奎为第一作者,张志超教授、王紫千副教授为通讯作者。
论文链接:https://www.sciencedirect.com/science/article/pii/S0168365926002300
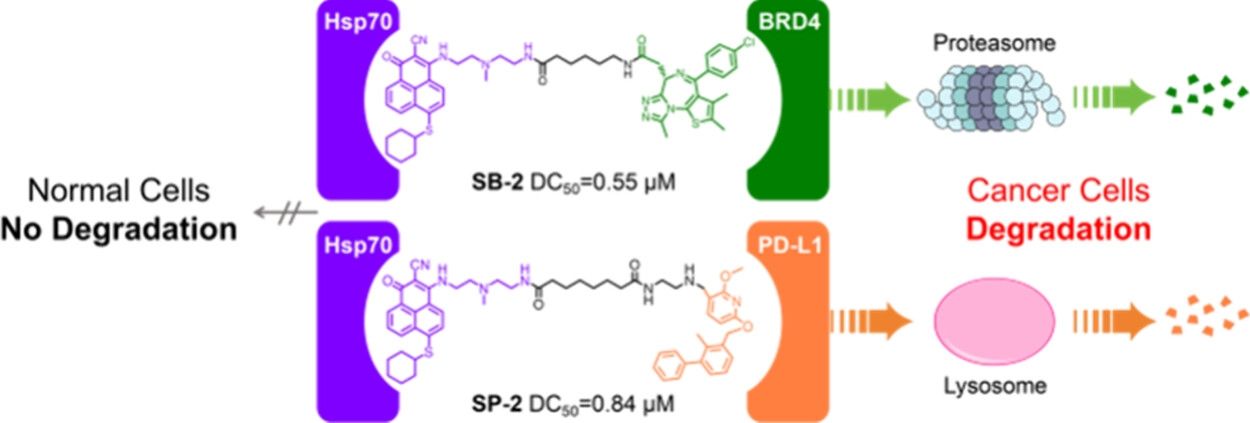
图2. HSP70TAC的机制示意图
基于HSP70的“双通路”肿瘤特异性蛋白靶向降解嵌合体(HSP70TAC)系统,实现单平台对胞内外蛋白的全域降解覆盖,避免了高浓度下三元复合物解离导致的“钩状效应”,保持高效降解。同样,利用Hsp70在肿瘤细胞中高表达的特征,Hsp70TAC也能够实现对靶蛋白的肿瘤特异性降解,降低正常细胞毒性。相关成果以“靶向Hsp70的嵌合体通过蛋白酶体和溶酶体同时降解细胞内外的蛋白质”(Hsp70-Targeting Chimeras Enable Dual Proteasomal and Lysosomal Degradation of Intracellular and Extracellular Proteins)为题发表于《药物化学杂志》(Journal of Medicinal Chemistry),我校医学部硕士生王子涵为第一作者,张志超教授、王紫千副教授为通讯作者。
论文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c03784
上述工作得到了国家自然科学基金面上项目、大连理工大学基础研究挂帅揭榜项目、大连理工大学-附属中心医院、附属肿瘤医院、附属第三人民医院等医工合作项目的资助。
来源:医学部
编辑:常思萌
 最新动态
最新动态