 2026-04-10
2026-04-10
近日,生物工程学院智能生物制造教育部重点实验室基因编辑与合成生物工程研究室刘嵘明教授团队在生化与分子生物学领域国际权威Top期刊《核酸研究》(Nucleic Acids Research)发表题为基于“PE-STAR:通过SOS应答触发和RecJ增强修复可在大肠杆菌中实现高效编辑的先导编辑技术”(PE-STAR:prime editing with SOS-triggered andRecJ-augmented repair enables high-efficiency editing in Escherichia coli)的研究型文章。我校生物工程学院为第一单位,刘嵘明教授、梁丽亚副教授为本文的通讯作者,2023级硕士生段小燕为第一作者。
先导编辑是一种多功能的CRISPR基因组工程技术,可在不引入双链断裂(DSBs)或无需供体模板的情况下实现精确的DNA插入、缺失和替换。先导编辑技术自哺乳动物细胞中首次开发以来展现出广泛的编辑能力,并且相较于依赖DSBs的基因组编辑方法具有更低的细胞毒性。但其在细菌应用中面临显著局限性,编辑效率较低及片段编辑范围过小等问题。
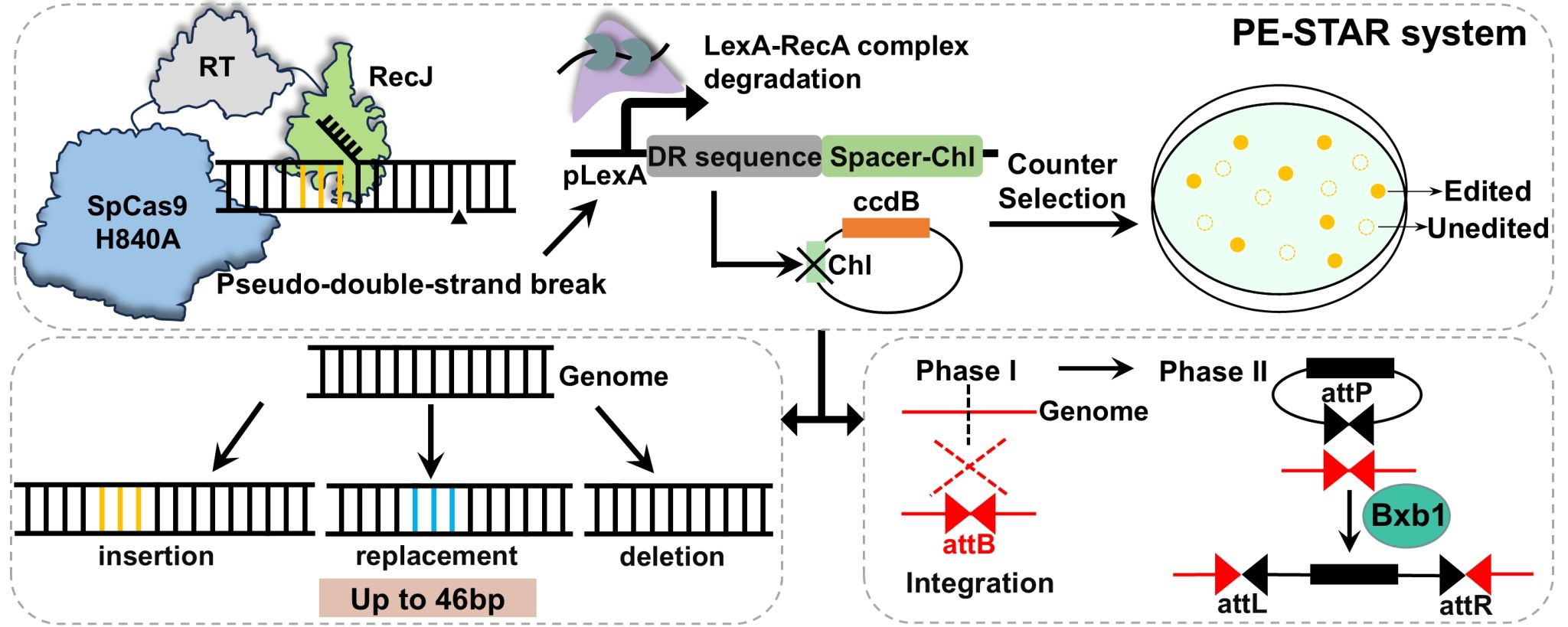
为此,团队开发了PE-STAR技术,即“SOS应答触发与RecJ增强修复的先导编辑技术”,以提高大肠杆菌中的基因编辑效率。这是一种整合了修复通路调控与SOS介导的筛选富集的一体化策略。敲除三个抑制性的3’→5’端核酸外切酶(SbcB、ExoX和XseA)提高了编辑链的保留率,并延长转化后的生长时间从而提高了编辑效率。RecJ的过表达增强了在缺口修复和间隙扩展过程中的5’端链方向的降解,使修复过程偏向逆转录整合产生的编辑链。为富集编辑成功的细胞,本研究整合了SOS响应性反向筛选回路,将PE3介导的双切口与依赖LexA的guide RNA(gRNA)表达关联,靶向编码毒素CcdB的质粒,从而消除未编辑的细胞。结果表明,PE-STAR在短片段修饰中实现了高达80%-90%的编辑效率,不同基因座间效率提升最高达16倍。该平台可高效支持长达46个碱基对(bp)的插入、删除及替换编辑。此外,通过PE-STAR技术构建attB位点并经Bxb1整合酶重组后,可在筛选菌落中实现3.2kb和8.0kb表达盒的染色体整合,包括GFP报告基因表达盒和核黄素生物合成途径,重组效率达100%。
PE-STAR为大肠杆菌提供了高效且无双链断裂的基因组工程平台,并为未来适应性改造提供了设计原则。本研究为拓展先导编辑技术在原核生物中的应用能力,以及加速生物制造、合成生物学和功能基因组学领域的菌株构建奠定了基础。
该研究得到了国家重点研发计划、青年教师科研创新能力支持计划、国家自然科学基金、“兴辽英才计划”项目、辽宁省自然科学基金、中央高校基本科研业务费专项资金等的支持。
来源:生物工程学院
编辑:程昕 常思萌
 最新动态
最新动态